Descrição de Motrin
O ingrediente ativo do MOTRIN é o ibuprofeno, que é membro do grupo do ácido propiônico dos antiinflamatórios não esteróides (AINEs). O ibuprofeno é uma mistura racêmica de [+]Areia [-]Enantiômeros R. É um pó cristalino branco a esbranquiçado, com ponto de fusão de 74° a 77°C. É praticamente insolúvel em água (<0,1 mg/mL), mas facilmente solúvel em solventes orgânicos como etanol e acetona. O ibuprofeno tem pKa de 4,43±0,03 e coeficiente de partição n-octanol/água de 11,7 em pH 7,4. O nome químico do ibuprofeno é ácido (±) -2- (p-isobutilfenil) propiônico. O peso molecular do ibuprofeno é 206,28. Sua fórmula molecular é C13H1802 e tem a seguinte fórmula estrutural:
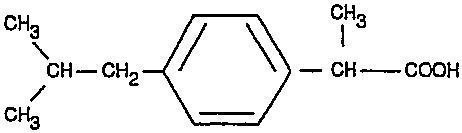
A suspensão MOTRIN é uma suspensão adoçada com sacarose, de cor laranja e com sabor de frutas vermelhas, contendo 100 mg de ibuprofeno em 5 mL (20 mg / mL). Os ingredientes inativos incluem: acessulfame-K, ácido cítrico, glicerina, polissorbato 80, amido pré-gelatinizado, água purificada, benzoato de sódio, sacarose, goma xantana e sabores naturais e artificiais. Também pode conter um ou vários dos seguintes corantes: FD&C Red #40, D&C Yellow #10, D&C Red #33 e FD&C Blue #1.
Motrin – Farmacologia Clínica
Farmacodinâmica – O ibuprofeno é um antiinflamatório não esteroidal (AINE) que possui atividade antiinflamatória, analgésica e antipirética. Seu modo de ação, como o de outros AINEs, não é completamente compreendido, mas pode estar relacionado à inibição da prostaglandina sintetase. Após a absorção do ibuprofeno racêmico, o [-]O enantiômero R sofre interconversão no [+]Forma S. As atividades biológicas do ibuprofeno estão associadas ao [+]Enantiômero S.
Farmacocinética – O ibuprofeno é uma mistura racêmica de [-]R-e [+]Isômeros S. Na Vivo e em vitro estudos indicam que [+]O isômero S é responsável pela atividade clínica. O [-]A forma R, embora considerada farmacologicamente inativa, é lenta e incompletamente (~60%) interconvertida na forma ativa [+]Espécies S em adultos. O grau de interconversão em crianças é desconhecido, mas acredita-se que seja semelhante. O [-]O isômero R serve como reservatório circulante para manter os níveis do fármaco ativo. O ibuprofeno é bem absorvido por via oral, sendo menos de 1% excretado inalterado na urina. Possui curva de tempo de eliminação bifásica com meia-vida plasmática de aproximadamente 2 horas. Estudos em crianças febris estabeleceram a proporcionalidade da dose de doses de 5 e 10 mg/kg de ibuprofeno. Estudos em adultos estabeleceram a proporcionalidade da dose de ibuprofeno como dose oral única de 50 a 600 mg para o medicamento total e até 1200 mg para o medicamento livre.
Absorção – Na Vivo estudos indicam que o ibuprofeno é bem absorvido por via oral a partir da formulação em suspensão, com níveis plasmáticos máximos geralmente ocorrendo dentro de 1 a 2 horas (ver Tabela 1).
| Dose | 200mg (2,8mg/kg) em Adultos |
10mg/kg em febril Crianças |
|
|---|---|---|---|
| Formulação | Suspensão | Suspensão | |
| Lenda: | AUCinf = Área sob a curva até o infinito | ||
| Tmax = Tempo até o pico da concentração plasmática | |||
| Cmax = concentração plasmática máxima | |||
| Cl/F = depuração dividida pela fração na absorção do medicamento | |||
| Número de pacientes | 24 | 18 | |
| AUCinf (μg•h/mL) | 64 (27%) |
155 (24%) |
|
| Cmáx (μg/mL) | 19 (22%) |
55 (23%) |
|
| Tmáx (h) | 0,79 (69%) |
0,97 (57%) |
|
| CI/F(mL/h/kg) | 45,6 (22%) |
68,6 (22%) |
|
Antiácidos – Um estudo de biodisponibilidade em adultos demonstrou que não houve interferência na absorção do ibuprofeno quando administrado em conjunto com um antiácido contendo hidróxido de alumínio e hidróxido de magnésio.
Antagonistas H-2– Em estudos com voluntários humanos, a administração concomitante de cimetidina ou ranitidina com ibuprofeno não teve efeito substantivo nas concentrações séricas de ibuprofeno.
Efeitos Alimentares – A absorção é mais rápida quando MOTRIN é administrado em jejum. A administração de MOTRIN Suspension com alimentos afeta a taxa, mas não a extensão da absorção. Quando tomado com alimentos, Tmáx. é atrasado em aproximadamente 30 a 60 minutos e os níveis de pico são reduzidos em aproximadamente 30 a 50%.
Distribuição – O ibuprofeno, como a maioria dos medicamentos de sua classe, liga-se fortemente às proteínas (>99% de ligação aos 20 μg/mL). A ligação às proteínas é saturável e em concentrações >20 μa ligação g/mL não é linear. Com base nos dados de dosagem oral, existe uma alteração no volume de distribuição do ibuprofeno relacionada com a idade ou a febre. Crianças febris <11 anos apresentam volume de aproximadamente 0,2 L/kg enquanto adultos apresentam volume de aproximadamente 0,12 L/kg. O significado clínico destes resultados é desconhecido.
Metabolismo – Após administração oral, a maior parte da dose foi recuperada na urina em 24 horas como metabólitos do ácido hidroxi-(25%) e carboxipropil-(37%) do ácido fenilpropiônico. As porcentagens de ibuprofeno livre e conjugado encontradas na urina foram de aproximadamente 1% e 14%, respectivamente. O restante da droga foi encontrado nas fezes como metabólitos e droga não absorvida.
Eliminação – O ibuprofeno é rapidamente metabolizado e eliminado na urina. A excreção do ibuprofeno está virtualmente completa 24 horas após a última dose. Possui curva de tempo de eliminação plasmática bifásica com meia-vida de aproximadamente 2,0 horas. Não há diferença na taxa de eliminação terminal observada ou na meia-vida entre crianças e adultos; no entanto, há uma alteração na depuração total relacionada à idade ou à febre. Isto sugere que a alteração observada na depuração se deve a alterações no volume de distribuição do ibuprofeno (ver Tabela 1 para valores de Cl/F).
Estudos clínicos – Ensaios clínicos controlados comparando doses de 5 e 10 mg/kg de suspensão de ibuprofeno e 10-15 mg/kg de elixir de paracetamol foram realizados em crianças de 6 meses a 12 anos de idade com febre principalmente devido a doenças virais. Nestes estudos não houve diferenças entre os tratamentos na redução da febre durante a primeira hora e a redução máxima da febre ocorreu entre 2 e 4 horas. A resposta após 1 hora dependeu tanto do nível de elevação da temperatura como do tratamento. Em crianças com temperaturas basais iguais ou inferiores a 102,5°F, ambas as doses de ibuprofeno e paracetamol foram igualmente eficazes em seu efeito máximo. Em crianças com temperaturas acima de 102,5°F, a dose de ibuprofeno 10 mg/kg foi mais eficaz. Às 6 horas, as crianças tratadas com ibuprofeno 5 mg/kg tenderam a ter recorrência da febre, enquanto as crianças tratadas com ibuprofeno 10 mg/kg ainda tiveram redução significativa da febre às 8 horas. Nos grupos de controle tratados com 10 mg/kg de paracetamol, a redução da febre foi semelhante à observada em crianças tratadas com 5 mg/kg de ibuprofeno, com a exceção de que a elevação da temperatura tendeu a retornar 1-2 horas antes.
Em pacientes com dismenorreia primária, foi demonstrado que o ibuprofeno reduz os níveis elevados de atividade das prostaglandinas no fluido menstrual e reduz os testes e a pressão intrauterina ativa, bem como a frequência das contrações uterinas. O provável mecanismo de ação é inibir a síntese de prostaglandinas, em vez de simplesmente fornecer analgesia.
Indicações e uso de Motrin
Considere cuidadosamente os benefícios e riscos potenciais da suspensão MOTRIN e outras opções de tratamento antes de decidir usar a suspensão MOTRIN. Use a dose eficaz mais baixa pelo menor período de tempo consistente com os objetivos individuais do tratamento do paciente (ver AVISOS).
Em pacientes pediátricos, a suspensão de MOTRIN é indicada:
- Para redução da febre em pacientes de 6 meses a 2 anos de idade.
- Para alívio da dor leve a moderada em pacientes de 6 meses a 2 anos de idade.
- Para alívio dos sinais e sintomas da artrite juvenil.
Em Adultos, MOTRIN está indicado:
- Para tratamento da dismenorreia primária.
- Para alívio dos sinais e sintomas da artrite reumatóide e osteoartrite.
Como não houve ensaios controlados para demonstrar se existe algum efeito benéfico ou interação prejudicial com o uso de ibuprofeno em conjunto com aspirina, a combinação não pode ser recomendada. (Ver PRECAUÇÕES – Interações medicamentosas).
Contra-indicações
A suspensão MOTRIN está contra-indicada em pacientes com hipersensibilidade conhecida ao ibuprofeno.
A suspensão de MOTRIN não deve ser administrada a pacientes que apresentaram asma, urticária ou reações alérgicas após tomar aspirina ou outros AINEs. Reações anafiláticas graves, raramente fatais, aos AINEs foram relatadas nesses pacientes (ver ADVERTÊNCIAS – Reações Anafilactóides, e PRECAUÇÕES – Asma pré-existente).
A suspensão de MOTRIN é contra-indicada para o tratamento da dor perioperatória no contexto de cirurgia de revascularização miocárdica (CABG) (ver AVISOS).
Avisos
EFEITOS CARDIOVASCULARES
Eventos Trombóticos Cardiovasculares
Ensaios clínicos de vários AINEs seletivos e não seletivos para COX-2 com duração de até três anos demonstraram um risco aumentado de eventos trombóticos cardiovasculares (CV) graves, infarto do miocárdio e acidente vascular cerebral, que podem ser fatais. Todos os AINEs, tanto seletivos quanto não seletivos para COX-2, podem apresentar um risco semelhante. Pacientes com doença CV conhecida ou fatores de risco para doença CV podem estar em maior risco. Para minimizar o risco potencial de um acontecimento CV adverso em doentes tratados com um AINE, deve ser utilizada a dose eficaz mais baixa durante o menor período possível. Médicos e pacientes devem permanecer alertas para o desenvolvimento de tais eventos, mesmo na ausência de sintomas cardiovasculares prévios. Os pacientes devem ser informados sobre os sinais e/ou sintomas de eventos cardiovasculares graves e as medidas a serem tomadas caso eles ocorram.
Não há evidências consistentes de que o uso concomitante de aspirina reduza o risco aumentado de eventos trombóticos cardiovasculares graves associados ao uso de AINEs. O uso concomitante de aspirina e um AINE aumenta o risco de eventos gastrointestinais graves (ver AVISOS IG).
Dois grandes ensaios clínicos controlados de um AINE seletivo para COX-2 para o tratamento da dor nos primeiros 10-14 dias após a cirurgia de revascularização do miocárdio encontraram um aumento na incidência de infarto do miocárdio e acidente vascular cerebral (ver CONTRA-INDICAÇÕES).
Hipertensão
Os AINEs, incluindo a suspensão de MOTRIN, podem levar ao aparecimento de nova hipertensão ou ao agravamento da hipertensão pré-existente, qualquer um dos quais pode contribuir para o aumento da incidência de eventos CV. Pacientes que tomam tiazidas ou diuréticos de alça podem ter resposta prejudicada a essas terapias quando tomam AINEs. Os AINEs, incluindo a suspensão MOTRIN, devem ser usados com cautela em pacientes com hipertensão. A pressão arterial (PA) deve ser monitorada de perto durante o início do tratamento com AINEs e durante todo o tratamento.
Insuficiência Cardíaca Congestiva e Edema
Retenção de líquidos e edema foram observados em alguns pacientes que tomam AINEs. A suspensão MOTRIN deve ser usada com cautela em pacientes com retenção de líquidos ou insuficiência cardíaca.
Efeitos gastrointestinais – Risco de ulceração, sangramento e perfuração
Os AINEs, incluindo a suspensão de MOTRIN, podem causar eventos adversos gastrointestinais (GI) graves, incluindo inflamação, sangramento, ulceração e perfuração do estômago, intestino delgado ou intestino grosso, que podem ser fatais. Estes eventos adversos graves podem ocorrer a qualquer momento, com ou sem sintomas de alerta, em pacientes tratados com AINEs. Apenas um em cada cinco pacientes que desenvolvem um evento adverso grave no trato gastrointestinal superior durante a terapia com AINEs é sintomático. Úlceras gastrointestinais superiores, sangramento grave ou perfuração causada por SN A AIDS ocorre em aproximadamente 1% dos pacientes tratados durante 3-6 meses e em cerca de 2-4% dos pacientes tratados durante um ano. Estas tendências continuam com uma utilização mais prolongada, aumentando a probabilidade de desenvolvimento de um evento GI grave em algum momento durante o curso da terapia. No entanto, mesmo a terapia de curto prazo apresenta riscos.
Os AINEs devem ser prescritos com extrema cautela em pessoas com história prévia de úlcera ou sangramento gastrointestinal. Pacientes com história prévia de úlcera péptica e/ou sangramento gastrointestinal que usam AINEs têm um risco maior que 10 vezes de desenvolver sangramento gastrointestinal em comparação com pacientes sem nenhum desses fatores de risco. Outros fatores que aumentam o risco de sangramento gastrointestinal em pacientes tratados com AINEs incluem o uso concomitante de corticosteróides orais ou anticoagulantes, maior duração da terapia com AINEs, tabagismo, uso de álcool, idade avançada e mau estado geral de saúde. A maioria das notificações espontâneas de acontecimentos gastrointestinais fatais ocorre em doentes idosos ou debilitados e, portanto, deve ter-se especial cuidado no tratamento desta população.
Para minimizar o risco potencial de um acontecimento GI adverso em doentes tratados com um AINE, deve ser utilizada a dose eficaz mais baixa durante o menor período possível. Pacientes e médicos devem permanecer alertas para sinais e sintomas de ulceração e sangramento GI durante a terapia com AINEs e iniciar imediatamente avaliação e tratamento adicionais se houver suspeita de um evento adverso GI grave. Isto deve incluir a descontinuação do AINE até que um evento adverso GI grave seja descartado. Para pacientes de alto risco, devem ser consideradas terapias alternativas que não envolvam AINEs.
Efeitos renais
A administração prolongada de AINEs resultou em necrose papilar renal e outras lesões renais. A toxicidade renal também foi observada em pacientes nos quais as prostaglandinas renais desempenham um papel compensatório na manutenção da perfusão renal. Nestes pacientes, a administração de um medicamento anti-inflamatório não esteróide pode causar uma redução dose-dependente na formação de prostaglandinas e, secundariamente, no fluxo sanguíneo renal, o que pode precipitar uma descompensação renal evidente. Os pacientes com maior risco desta reação são aqueles com função renal comprometida, insuficiência cardíaca, disfunção hepática, aqueles que tomam diuréticos e inibidores da ECA e idosos. A descontinuação da terapia com AINEs é geralmente seguida pela recuperação ao estado pré-tratamento.
Doença Renal Avançada
Nenhuma informação está disponível em estudos clínicos controlados sobre o uso de suspensão de MOTRIN em pacientes com doença renal avançada. Portanto, o tratamento com suspensão MOTRIN não é recomendado nestes pacientes com doença renal avançada. Se a terapia com suspensão de MOTRIN precisar ser iniciada, é aconselhável monitorar de perto a função renal do paciente.
Reações Anafilactóides
Tal como acontece com outros AINEs, podem ocorrer reações anafilactóides em pacientes sem exposição prévia conhecida à suspensão de MOTRIN. A suspensão de MOTRIN não deve ser administrada a pacientes com a tríade da aspirina. Este complexo de sintomas geralmente ocorre em pacientes asmáticos que apresentam rinite com ou sem pólipos nasais, ou que apresentam broncoespasmo grave e potencialmente fatal após tomar aspirina ou outros AINEs (ver CONTRA-INDICAÇÕES e PRECAUÇÕES – Asma pré-existente). A ajuda de emergência deve ser procurada nos casos em que ocorre uma reação anafilactóide.
Reações cutâneas
Os AINEs, incluindo a suspensão de MOTRIN, podem causar eventos adversos graves na pele, como dermatite esfoliativa, síndrome de Stevens-Johnson (SSJ) e necrólise epidérmica tóxica (NET), que pode ser fatal. Esses eventos graves podem ocorrer sem aviso prévio. Os pacientes devem ser informados sobre os sinais e sintomas de manifestações cutâneas graves e o uso do medicamento deve ser interrompido ao primeiro aparecimento de erupção cutânea ou qualquer outro sinal de hipersensibilidade.
Gravidez
No final da gravidez, tal como acontece com outros AINEs, MOTRIN deve ser evitado porque pode causar encerramento prematuro do canal arterial.
Precauções
Em geral
Não se pode esperar que a suspensão de MOTRIN substitua os corticosteróides ou trate a insuficiência de corticosteróides. A interrupção abrupta dos corticosteróides pode levar à exacerbação da doença. Pacientes em terapia prolongada com corticosteróides devem ter sua terapia reduzida lentamente se for tomada a decisão de descontinuar os corticosteróides.
A atividade farmacológica da suspensão de MOTRIN na redução da febre e da inflamação pode diminuir a utilidade desses sinais diagnósticos na detecção de complicações de condições dolorosas e não infecciosas presumidas.
Efeitos hepáticos
Elevações limítrofes de um ou mais testes hepáticos podem ocorrer em até 15% dos pacientes que tomam AINEs, incluindo suspensão de MOTRIN. Estas anomalias laboratoriais podem progredir, permanecer inalteradas ou podem ser transitórias com a continuação da terapêutica. Elevações notáveis de ALT ou AST (aproximadamente três ou mais vezes o limite superior do normal) foram relatadas em aproximadamente 1% dos pacientes em ensaios clínicos com AINEs. Além disso, foram relatados casos raros de reações hepáticas graves, incluindo icterícia e hepatite fulminante fatal, necrose hepática e insuficiência hepática, algumas delas com resultados fatais.
Um paciente com sintomas e/ou sinais sugestivos de disfunção hepática, ou no qual ocorreu um teste hepático anormal, deve ser avaliado quanto a evidências de desenvolvimento de uma reação hepática mais grave durante o tratamento com suspensão de MOTRIN. Se ocorrerem sinais e sintomas clínicos consistentes com doença hepática ou se ocorrerem manifestações sistêmicas (por exemplo, eosinofilia, erupção cutânea, etc.), a suspensão de MOTRIN deve ser descontinuada.
Efeitos hematológicos
Às vezes, a anemia é observada em pacientes que recebem AINEs, incluindo a suspensão de MOTRIN. Isto pode ser devido à retenção de líquidos, perda de sangue gastrointestinal oculta ou grave ou a um efeito descrito de forma incompleta sobre a eritropoiese. Pacientes em tratamento prolongado com AINEs, incluindo suspensão de MOTRIN, devem ter sua hemoglobina ou hematócrito verificados se apresentarem quaisquer sinais ou sintomas de anemia.
Em dois estudos clínicos pós-comercialização, a incidência de diminuição do nível de hemoglobina foi maior do que o relatado anteriormente. Uma diminuição na hemoglobina de 1 grama ou mais foi observada em 17,1% dos 193 pacientes que receberam 1.600 mg de ibuprofeno diariamente (osteoartrite) e em 22,8% dos 189 pacientes que tomaram 2.400 mg de ibuprofeno diariamente (artrite reumatóide). Testes de sangue oculto nas fezes positivos e níveis elevados de creatinina sérica também foram observados nestes estudos.
Os AINEs inibem a agregação plaquetária e demonstraram prolongar o tempo de sangramento em alguns pacientes. Ao contrário da aspirina, o seu efeito sobre a função plaquetária é quantitativamente menor, de menor duração e reversível. Pacientes recebendo suspensão de MOTRIN que possam ser afetados adversamente por alterações na função plaquetária, como aqueles com distúrbios de coagulação ou pacientes recebendo anticoagulantes, devem ser cuidadosamente monitorados.
Asma pré-existente
Pacientes com asma podem ter asma sensível à aspirina. O uso de aspirina em pacientes com asma sensível à aspirina tem sido associado a broncoespasmo grave, que pode ser fatal. Como foi relatada reatividade cruzada, incluindo broncoespasmo, entre aspirina e outros antiinflamatórios não esteróides em pacientes sensíveis à aspirina, a suspensão de MOTRIN não deve ser administrada a pacientes com esta forma de sensibilidade à aspirina e deve ser usada com cautela em pacientes com pré-existente asma.
Meningite Asséptica
Meningite asséptica, com febre e coma, foi observada em raras ocasiões em pacientes em terapia com ibuprofeno. Embora seja provavelmente mais provável de ocorrer em pacientes com lúpus eritematoso sistêmico e doenças relacionadas do tecido conjuntivo, foi relatado em pacientes que não apresentam doença crônica subjacente.
Diabéticos
A suspensão MOTRIN contém 0,3 g de sacarose e 1,6 calorias por mL, ou 1,5 g de sacarose e 8 calorias por colher de chá, o que deve ser levado em consideração no tratamento de pacientes diabéticos com este produto.
Informações para pacientes:
Os pacientes devem ser informados das seguintes informações antes de iniciar a terapia com um AINE e periodicamente durante o curso da terapia em andamento. Os pacientes também devem ser incentivados a ler o Guia de Medicamentos AINE que acompanha cada prescrição dispensada.
- A suspensão de MOTRIN, como outros AINEs, pode causar efeitos colaterais CV graves, como infarto do miocárdio ou acidente vascular cerebral, que podem resultar em hospitalização e até morte. Embora eventos CV graves possam ocorrer sem sintomas de alerta, os pacientes devem estar alertas para os sinais e sintomas de dor no peito, falta de ar, fraqueza, fala arrastada e devem procurar orientação médica ao observar qualquer sinal ou sintoma indicativo. Os pacientes devem ser informados da importância deste acompanhamento (ver ADVERTÊNCIAS, Efeitos Cardiovasculares).
- A suspensão de MOTRIN, como outros AINEs, pode causar desconforto gastrointestinal e, raramente, efeitos colaterais gastrointestinais graves, como úlceras e sangramento, que podem resultar em hospitalização ou até morte. Embora ulcerações e sangramentos graves do trato gastrointestinal possam ocorrer sem sintomas de aviso, os pacientes devem estar alertas para sinais e sintomas de ulcerações e sangramento, e devem procurar orientação médica ao observar qualquer sinal ou sintoma indicativo, incluindo dor epigástrica, dispepsia, melena e hematêmese. Os pacientes devem ser informados da importância deste acompanhamento (ver ADVERTÊNCIAS, efeitos gastrointestinais: risco de ulceração, sangramento e perfuração).
- A suspensão de MOTRIN, como outros AINEs, pode causar efeitos colaterais graves na pele, como dermatite esfoliativa, SSJ e RTE, que podem resultar em hospitalizações e até morte. Embora possam ocorrer reações cutâneas graves sem aviso prévio, os doentes devem estar atentos aos sinais e sintomas de erupção cutânea e bolhas, febre ou outros sinais de hipersensibilidade, como comichão, e devem consultar um médico quando observarem quaisquer sinais ou sintomas indicativos. Os pacientes devem ser aconselhados a interromper o medicamento imediatamente se desenvolverem qualquer tipo de erupção cutânea ou entrar em contato com o médico o mais rápido possível.
- Os pacientes devem relatar imediatamente aos seus médicos sinais e sintomas de ganho de peso inexplicável ou edema.
- Os pacientes devem ser informados sobre os sinais e sintomas de alerta de hepatotoxicidade (por exemplo, náusea, fadiga, letargia, prurido, icterícia, sensibilidade no quadrante superior direito e sintomas “semelhantes aos da gripe”). Se isto ocorrer, os pacientes devem ser instruídos a interromper a terapia e procurar terapia médica imediata.
- Os doentes devem ser informados dos sinais de uma reação anafilactóide (por exemplo, dificuldade em respirar, inchaço da face ou garganta). Se isto ocorrer, os pacientes devem ser instruídos a procurar ajuda de emergência imediata (ver AVISOS).
- No final da gravidez, tal como acontece com outros AINEs, a suspensão de MOTRIN deve ser evitada porque pode causar encerramento prematuro do canal arterial.
Testes laboratoriais
Como podem ocorrer ulcerações e sangramentos graves do trato gastrointestinal sem sintomas de alerta, os médicos devem monitorar sinais ou sintomas de sangramento gastrointestinal. Pacientes em tratamento prolongado com AINEs devem ter seu hemograma completo e um perfil químico verificados periodicamente. Se ocorrerem sinais e sintomas clínicos consistentes com doença hepática ou renal, ocorrerão manifestações sistêmicas (por exemplo, eosinofilia, erupção cutânea, etc.) ou se testes hepáticos anormais persistirem ou piorarem, a suspensão de MOTRIN deve ser descontinuada.
Interações medicamentosas
Inibidores da ECA
Os relatórios sugerem que os AINEs podem diminuir o efeito anti-hipertensivo dos inibidores da ECA. Esta interação deve ser considerada em pacientes que tomam AINEs concomitantemente com inibidores da ECA.
Aspirina
Tal como acontece com outros AINEs, a administração concomitante de ibuprofeno e aspirina geralmente não é recomendada devido ao potencial de aumento de efeitos adversos.
Diuréticos
Estudos clínicos, bem como observações pós-comercialização, demonstraram que a suspensão de MOTRIN pode reduzir o efeito natriurético da furosemida e das tiazidas em alguns pacientes. Esta resposta foi atribuída à inibição da síntese renal de prostaglandinas. Durante a terapia concomitante com AINEs, o paciente deve ser observado atentamente quanto a sinais de insuficiência renal (ver ADVERTÊNCIAS, efeitos renais), bem como para garantir eficácia diurética.
Lítio
O ibuprofeno produziu uma elevação dos níveis plasmáticos de lítio e uma redução na depuração renal do lítio em um estudo com onze voluntários normais. A concentração média mínima de lítio aumentou 15% e a depuração renal do lítio diminuiu 19% durante este período de administração concomitante do medicamento. Este efeito foi atribuído à inibição da síntese renal de prostaglandinas pelo ibuprofeno. Assim, quando MOTRIN e lítio são administrados concomitantemente, os indivíduos devem ser cuidadosamente observados quanto a sinais de toxicidade por lítio. (Leia as circulares sobre a preparação de lítio antes de usar essa terapia concomitante.)
Metotrexato
Foi relatado que os AINEs inibem competitivamente o acúmulo de metotrexato em fatias de rim de coelho. Isto pode indicar que podem aumentar a toxicidade do metotrexato. Deve-se ter cautela quando AINEs são administrados concomitantemente com metotrexato.
Varfarina
Vários estudos controlados de curto prazo não conseguiram demonstrar que os comprimidos de MOTRIN afetaram significativamente os tempos de protrombina ou uma variedade de outros fatores de coagulação quando administrados a indivíduos em uso de anticoagulantes do tipo varfarina. No entanto, como foi relatado sangramento quando comprimidos de MOTRIN e outros AINEs foram administrados a pacientes em uso de anticoagulantes do tipo varfarina, o médico deve ser cauteloso ao administrar comprimidos de MOTRIN a pacientes em uso de anticoagulantes. Os efeitos da varfarina e dos AINEs no sangramento gastrointestinal são sinérgicos, de modo que os usuários de ambos os medicamentos em conjunto apresentam um risco de sangramento gastrointestinal grave maior do que os usuários de qualquer um dos medicamentos isoladamente.
Gravidez
Efeitos teratogênicos – categoria C de gravidez
Estudos reprodutivos realizados em ratos e coelhos não demonstraram evidências de anomalias no desenvolvimento. No entanto, os estudos de reprodução animal nem sempre são preditivos da resposta humana. Não existem estudos adequados e bem controlados em mulheres grávidas. Motrin deve ser usado durante a gravidez apenas se o benefício potencial justificar o risco potencial para o feto.
Efeitos não teratogênicos
Devido aos efeitos conhecidos dos anti-inflamatórios não esteróides no sistema cardiovascular fetal (fechamento do canal arterial), o uso durante a gravidez (particularmente no final da gravidez) deve ser evitado.
Trabalho e entrega
Em estudos em ratos com AINEs, assim como com outros medicamentos conhecidos por inibir a síntese de prostaglandinas, ocorreu um aumento na incidência de distocia, atraso no parto e diminuição da sobrevivência dos filhotes. Os efeitos da suspensão de MOTRIN no trabalho de parto e parto em mulheres grávidas são desconhecidos. Portanto, a administração de suspensão MOTRIN não é recomendada durante o trabalho de parto e parto.
Mães que amamentam
Não se sabe se este medicamento é excretado no leite humano. Como muitos medicamentos são excretados no leite humano e devido ao potencial de reações adversas graves em lactentes decorrentes da suspensão de MOTRIN, deve-se tomar uma decisão sobre a descontinuação da amamentação ou a descontinuação do medicamento, levando em consideração a importância do medicamento para a mãe. .
Uso Pediátrico
A segurança e eficácia da suspensão de MOTRIN em pacientes pediátricos com idade inferior a 6 meses não foram estabelecidas (ver FARMACOLOGIA CLÍNICA – Estudos Clínicos). A dosagem da suspensão de MOTRIN em crianças com 6 meses ou mais deve ser orientada pelo peso corporal (ver DOSAGEM E ADMINISTRAÇÃO).
Uso Geriátrico
Tal como acontece com qualquer AINE, deve-se ter cautela no tratamento de idosos (65 anos ou mais).
Reações adversas/efeitos colaterais
Em pacientes que tomam MOTRIN ou outros AINEs, as experiências adversas relatadas com mais frequência que ocorrem em aproximadamente 1-10% dos pacientes são: Função renal anormal, anemia, tontura, edema, enzimas hepáticas elevadas, retenção de líquidos, experiências gastrointestinais (incluindo dor abdominal, distensão abdominal , prisão de ventre, diarréia, dispepsia, dor epigástrica, flatulência, azia, náusea, vômito), dores de cabeça, aumento do tempo de sangramento, nervosismo, prurido, erupções cutâneas (incluindo maculopapular) e zumbido.
| Experiências adversas adicionais relatadas ocasionalmente incluem: | |
| Corpo como um todo – | febre, infecção, sepse |
| Sistema cardiovascular – | insuficiência cardíaca congestiva em pacientes com função cardíaca marginal, hipertensão, taquicardia, síncope |
| Sistema digestivo – | boca seca, duodenite, esofagite, úlcera gástrica ou duodenal com sangramento e/ou perfuração, gastrite, sangramento gastrointestinal, glossite, hematêmese, hepatite, icterícia, melena, sangramento retal |
| Sistema hemico e linfático – | equimose, eosinofilia, leucopenia, púrpura, estomatite, trombocitopenia |
| Metabólico e nutricional – | mudanças de peso |
| Sistema nervoso – | ansiedade, astenia, confusão, depressão, anomalias nos sonhos, sonolência, insónia, mal-estar, parestesia, sonolência, tremores, vertigens |
| Sistema respiratório – | asma, dispneia |
| Pele e anexos – | alopecia, fotossensibilidade, suor |
| Sentidos especiais – | visão embaçada |
| Sistema urogenital – | cistite, disúria, hematúria, nefrite intersticial, oligúria/poliúria, proteinúria, insuficiência renal aguda em pacientes com função renal significativamente comprometida pré-existente |
| Outras reações adversas, que ocorrem raramente são: | |
| Corpo como um todo – | reações anafiláticas, reações anafilactóides, alterações do apetite, |
| Sistema cardiovascular – | arritmia, acidente vascular cerebral, hipotensão, enfarte do miocárdio, palpitações, vasculite |
| Sistema digestivo – | eructação, úlcera gengival, síndrome hepatorrenal, necrose hepática, insuficiência hepática, pancreatite |
| Sistema hemico e linfático – | agranulocistose, anemia hemolítica, anemia aplástica, linfadenopatia, neutropenia, pancitopenia |
| Metabólico e nutricional – | hiperglicemia |
| Sistema nervoso – | convulsões, coma, labilidade emocional, alucinações, meningite asséptica |
| Respiratório – | apneia, depressão respiratória, pneumonia, rinite |
| Pele e anexos – | angioedema, necrose epidérmica tóxica, eritema multiforme, dermatite esfoliativa, síndrome de Stevens Johnson, urticária, erupções vesiculobolhosas |
| Sentidos especiais – | ambliopia (visão turva e/ou diminuída, escotomas e/ou alterações na visão das cores), conjuntivite, olhos secos, deficiência auditiva |
| Urogenital- | azotemia, diminuição da depuração da creatinina, glomerulite, necrose papilar renal, necrose tubular |
Sobredosagem
A toxicidade da overdose de ibuprofeno depende da quantidade de medicamento ingerido e do tempo decorrido desde a ingestão, embora a resposta individual possa variar, o que torna necessária a avaliação de cada caso individualmente. Embora incomum, foram relatadas toxicidade grave e morte na literatura médica com superdosagem de ibuprofeno. Os sintomas mais frequentemente relatados de overdose de ibuprofeno incluem dor abdominal, náusea, vômito, letargia e sonolência. Outros sintomas do sistema nervoso central incluem dor de cabeça, zumbido, depressão do SNC e convulsões. Acidose metabólica, coma, insuficiência renal aguda e apneia (principalmente em crianças muito pequenas) podem ocorrer raramente. Toxicidade cardiovascular, incluindo hipotensão, bradicardia, taquicardia e fibrilação atrial, também foi relatada.
O tratamento da sobredosagem aguda com ibuprofeno é principalmente de suporte. Pode ser necessário o tratamento da hipotensão, acidose e hemorragia gastrointestinal. Em casos de sobredosagem aguda, o estômago deve ser esvaziado através de emese ou lavagem induzida por ipeca. A êmese é mais eficaz se iniciada 30 minutos após a ingestão. O carvão ativado administrado por via oral pode ajudar a reduzir a absorção e reabsorção do ibuprofeno.
Em crianças, a quantidade estimada de ibuprofeno ingerida por peso corporal pode ser útil para prever o potencial de desenvolvimento de toxicidade, embora cada caso deva ser avaliado. É improvável que a ingestão de menos de 100 mg/kg produza toxicidade. Crianças que ingerem 100 a 200 mg/kg podem ser tratadas com êmese induzida e um tempo mínimo de observação de quatro horas. Crianças que ingerem 200 a 400 mg/kg de ibuprofeno devem ter esvaziamento gástrico imediato e pelo menos quatro horas de observação em unidade de saúde. Crianças que ingerem mais de 400 mg/kg necessitam de encaminhamento médico imediato, observação cuidadosa e terapia de suporte apropriada. A êmese induzida por ipeca não é recomendada em sobredosagens superiores a 400 mg/kg devido ao risco de convulsões e ao potencial de aspiração do conteúdo gástrico.
Em pacientes adultos, o histórico da dose supostamente ingerida não parece ser preditivo de toxicidade. A necessidade de encaminhamento e acompanhamento deve ser avaliada pelas circunstâncias no momento da ingestão da overdose. Adultos sintomáticos devem ser cuidadosamente avaliados, observados e apoiados.
Dosagem e administração de Motrin
Considere cuidadosamente os benefícios e riscos potenciais da suspensão MOTRIN e outras opções de tratamento antes de decidir usar a suspensão MOTRIN. Use a dose eficaz mais baixa pelo menor período de tempo consistente com os objetivos individuais do tratamento do paciente (ver AVISOS).
Após observar a resposta à terapia inicial com suspensão de MOTRIN, a dose e a frequência devem ser ajustadas para atender às necessidades individuais do paciente.
PACIENTES PEDIÁTRICOS
Redução da febre: Para redução da febre em crianças de 6 meses a 2 anos de idade, a posologia deve ser ajustada com base no nível de temperatura inicial (ver FARMACOLOGIA CLÍNICA). A dose recomendada é de 5 mg/kg se a temperatura basal for inferior a 102,5ºF, ou 10 mg/kg se a temperatura basal for 102,5ºF ou superior. A duração da redução da febre é geralmente de 6 a 8 horas. A dose diária máxima recomendada é de 40 mg/kg.
Analgesia: Para alívio de dores leves a moderadas em crianças de 6 meses a 2 anos de idade, a dosagem recomendada é de 10 mg/kg, a cada 6 a 8 horas. A dose diária máxima recomendada é de 40 mg/kg. As doses devem ser administradas de forma a não perturbar o padrão de sono da criança.
Artrite Juvenil: A dose recomendada é de 30 a 40 mg/kg/dia dividida em três a quatro doses (ver Individualização da Posologia). Pacientes com doença mais leve podem ser tratados adequadamente com 20 mg/kg/dia.
Em pacientes com artrite juvenil, doses acima de 50 mg/kg/dia não são recomendadas porque não foram estudadas e doses que excedem a dose máxima recomendada de 40 mg/kg/dia podem aumentar o risco de causar eventos adversos graves. A resposta terapêutica pode levar de alguns dias a várias semanas para ser alcançada. Uma vez obtido o efeito clínico, a posologia deve ser reduzida para a menor dose de MOTRIN necessária para manter o controle adequado dos sintomas.
Pacientes pediátricos que recebem doses acima de 30 mg/kg/dia ou se ocorreram testes de função hepática anormais com tratamentos anteriores com AINEs devem ser cuidadosamente monitorados quanto a sinais e sintomas de disfunção hepática precoce.
ADULTOS
Dismenorreia Primária: Para o tratamento da dismenorreia primária, começando com o início mais precoce dessa dor, a Suspensão MOTRIN deve ser administrada na dose de 400 mg a cada 4 horas, conforme necessário, para o alívio da dor.
Artrite reumatóide e osteoartrite: Dosagem sugerida: 1.200-3.200 mg por dia (300 mg quatro vezes ao dia ou 400 mg, 600 mg ou 800 mg três vezes ao dia ou quatro vezes ao dia). Pacientes individuais podem apresentar uma melhor resposta a 3.200 mg por dia, em comparação com 2.400 mg, embora em ensaios clínicos bem controlados os pacientes que receberam 3.200 mg não tenham apresentado uma melhor resposta média em termos de eficácia. Portanto, ao tratar pacientes com 3.200 mg/dia, o médico deve observar benefícios clínicos aumentados o suficiente para compensar o risco potencial aumentado.
Individualização da Dosagem: A dose de suspensão de MOTRIN deve ser adaptada a cada paciente e pode ser reduzida ou aumentada em relação às doses sugeridas, dependendo da gravidade dos sintomas no momento do início da terapia medicamentosa ou à medida que o paciente responde ou não responde.
Um estudo sobre febre mostrou que, após a dose inicial de suspensão de MOTRIN, as doses subsequentes podem ser reduzidas e ainda fornecer controle adequado da febre.
Numa situação em que a febre baixa exigiria a dose de MOTRIN Suspensão 5 mg/kg em uma criança com dor, deve-se escolher a dose que tratará efetivamente o sintoma predominante.
Em condições crônicas, uma resposta terapêutica O uso de MOTRIN A terapia de suspensão às vezes é observada em alguns dias a uma semana, mas na maioria das vezes é observada em duas semanas. Depois de alcançada uma resposta satisfatória, a dose do paciente deve ser revista e ajustada conforme necessário.
Pacientes com artrite reumatóide parecem necessitar de doses mais elevadas do que pacientes com osteoartrite. Deve ser utilizada a menor dose de suspensão de MOTRIN que produza um controle aceitável.
A suspensão MOTRIN pode ser usada em combinação com sais de ouro e/ou corticosteróides.
Como o Motrin é fornecido
MOTRIN® (ibuprofeno) Suspensão, 100 mg/5 mL
Suspensão de cor laranja com sabor de frutas vermelhas
– Frascos de 120 mL – NDC 0045-0448-04
– Frascos de 480 mL – NDC 0045-0448-16
Agite bem antes de usar. Armazene em temperatura ambiente controlada [15º to 30ºC (59º to 86ºF)]
Cuidado: A Lei Federal proíbe a dispensação sem receita médica.
SAÚDE DO CONSUMIDOR McNEIL
DIVISÃO DE McNEIL-PPC, INC.
FORT WASHINGTON, PA 19034-EUA
Abril de 2009
Guia de medicação
(Consulte o final deste Guia de Medicamentos para obter uma lista de medicamentos AINE prescritos.)
Qual é a informação mais importante que devo saber sobre medicamentos chamados anti-inflamatórios não esteróides (AINEs)?
Os medicamentos AINE podem aumentar a probabilidade de ataque cardíaco ou acidente vascular cerebral que pode levar à morte. Essa chance aumenta:
- com uso mais prolongado de medicamentos AINE
- em pessoas que têm doenças cardíacas
Os medicamentos AINE nunca devem ser usados imediatamente antes ou depois de uma cirurgia cardíaca chamada “revascularização do miocárdio (CRM)”.
Os medicamentos AINE podem causar úlceras e hemorragias no estômago e intestinos a qualquer momento durante o tratamento. Úlceras e sangramento:
- pode acontecer sem sintomas de alerta
- pode causar a morte
A chance de uma pessoa ter úlcera ou sangramento aumenta com:
- tomar medicamentos chamados “corticosteroides” e “anticoagulantes”
- uso mais longo
- fumar
- beber álcool
- idoso
- tendo problemas de saúde
Os medicamentos AINE só devem ser usados:
- exatamente como prescrito
- na dose mais baixa possível para o seu tratamento
- pelo menor tempo necessário
O que são medicamentos antiinflamatórios não esteróides (AINEs)?
Os medicamentos AINE são usados para tratar dor e vermelhidão, inchaço e calor (inflamação) de condições médicas como:
- diferentes tipos de artrite
- cólicas menstruais e outros tipos de dor de curto prazo
Quem não deve tomar um medicamento antiinflamatório não esteroidal (AINE)?
Não tome um medicamento AINE:
- se você teve um ataque de asma, urticária ou outra reação alérgica com aspirina ou qualquer outro medicamento AINE
- para dor logo antes ou depois da cirurgia de ponte de safena
Informe o seu médico:
- sobre todas as suas condições médicas
- sobre todos os medicamentos que você toma. Os AINEs e alguns outros medicamentos podem interagir entre si e causar efeitos colaterais graves. Mantenha uma lista de seus medicamentos para mostrar ao seu médico e farmacêutico.
- se você estiver grávida. Os medicamentos AINE não devem ser utilizados por mulheres grávidas no final da gravidez.
- se você estiver amamentando. Fale com seu médico.
Quais são os possíveis efeitos colaterais dos antiinflamatórios não esteroidais (AINEs)?
Os efeitos colaterais graves incluem:
|
Outros efeitos colaterais incluem:
|
Obtenha ajuda de emergência imediatamente se tiver algum dos seguintes sintomas:
|
|
Pare o seu medicamento AINE e ligue imediatamente para o seu médico se tiver algum dos seguintes sintomas:
|
|
Estes não são todos os efeitos secundários dos medicamentos AINE. Fale com o seu médico ou farmacêutico para obter mais informações sobre os medicamentos AINE.
Outras informações sobre medicamentos antiinflamatórios não esteróides (AINEs)
- A aspirina é um medicamento AINE, mas não aumenta a chance de ataque cardíaco. A aspirina pode causar sangramento no cérebro, estômago e intestinos. A aspirina também pode causar úlceras no estômago e nos intestinos.
- Alguns destes medicamentos AINE são vendidos em doses mais baixas sem receita médica (sem receita). Converse com seu médico antes de usar AINEs vendidos sem receita médica por mais de 10 dias.
Medicamentos AINE que necessitam de receita médica
|
|
| Nome genérico | Nome comercial |
| Celecoxibe | Celebrex |
| Diclofenaco | Cataflam, Voltaren, Arthrotec (combinado com misoprostol) |
| Diflunisal | Dolobid |
| Etodolaco | Lodine, Lodine XL |
| Fenoprofeno | Nalfon, Nalfon 200 |
| Flurbirofeno | Ansaid |
| Ibuprofeno | Motrin, Tab-Profen, Vicoprofen* (combinado com hidrocodona), Combunox (combinado com oxicodona) |
| Indometacina | Indocin, Indocin SR, Indo-Lemmon, Indometagan |
| Cetoprofeno | Oruvail |
| Cetorolaco | Toradol |
| Ácido mefenâmico | Ponstel |
| Meloxicam | Móbico |
| Nabumetona | Relafen |
| Naproxeno | Naprosyn, Anaprox, Anaprox DS, EC-Naproxyn, Naprelan, Naprapac (embalado com lansoprazol) |
| Oxaprozina | Daypro |
| Piroxicam | Feldene |
| Sulindac | Clinoril |
| Tolmetina | Tolectina, Tolectina DS, Tolectina 600 |

